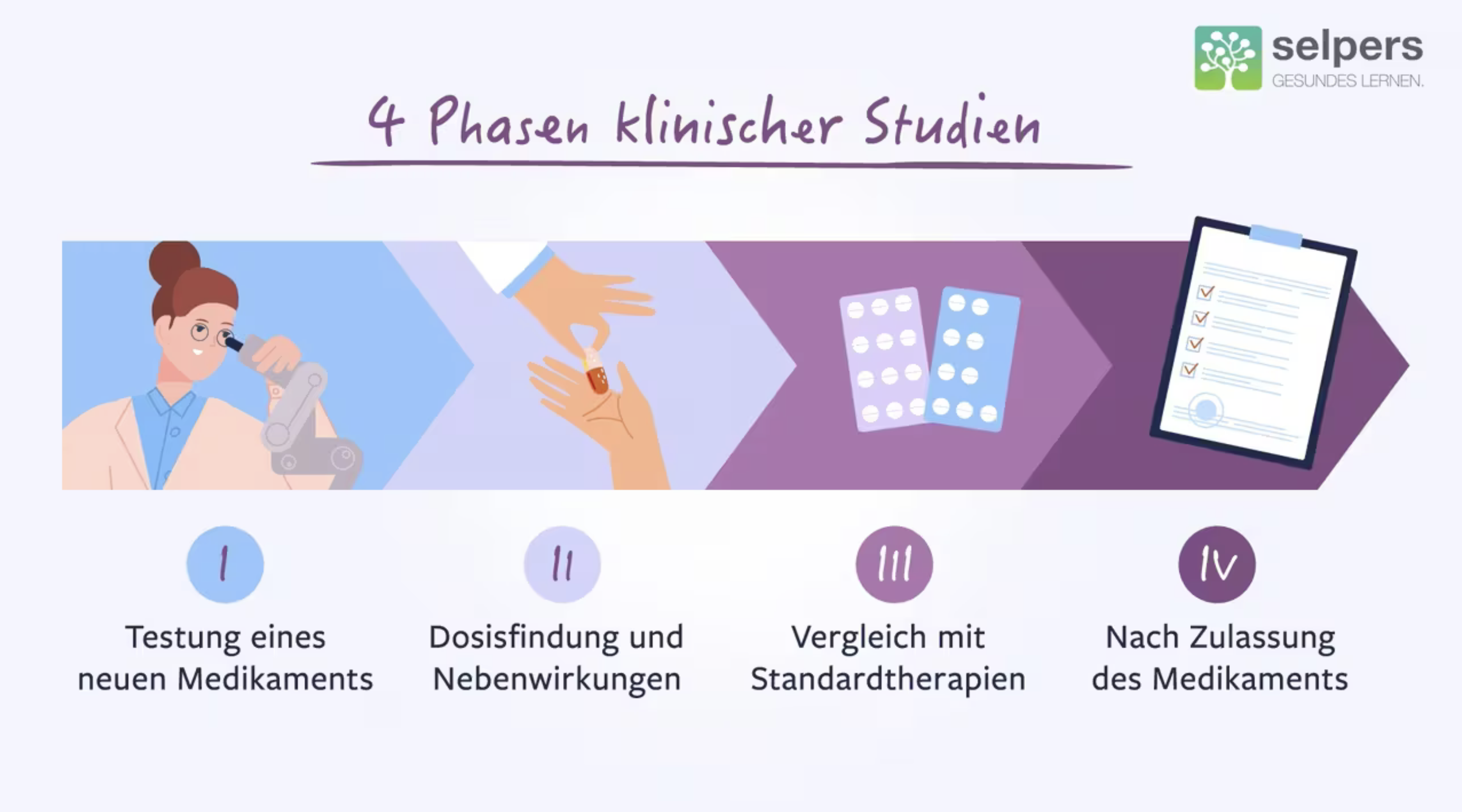
Eine klinische Studie dient dazu, ein bestimmtes, noch nicht öffentlich zugängliches Medikament oder Behandlungsverfahren auf dessen Sicherheit und Wirksamkeit zu prüfen.
Also: Wirkt dieses neue Medikament/die neue Methode?
Das kann z.B. ein Medikament sein, das einen neuen Wirkstoff enthält, aber auch eine neue Art ein Medikament zu verabreichen.
Es können aber auch zwei oder mehrere bereits zugelassene Medikamente miteinander verglichen werden.